اولین باتری را چه کسانی ساختند؟
در ابتدا ممکن است تصور کنید اولین باطری های ساخته شده در جهان قدمتی حدود 200 یا نهایتا 300 ساله دارد؛ اما این تاریخچه، مختص باتری های مدرن است. جالب است بدانید اولین باتریها را ایرانیان باستان (اشکانیها) اختراع کردند و هزاران سال قبل از کشف الکتریسیته از آن برای موارد صنعتی استفاده میکرده اند.
باتری اشکانیان (باطری پارتی) اولین باتری ساخته شده توسط انسان
از ابتدای قرن نوزدهم تا اواسط قرن بیستم، جهان الکساندر ولتا را به عنوان مخترع باتری می شناخت، اما کشفیات باستان شناسی در قرن بیستم نشان داد ایرانیان حدود 200 سال پیش از میلاد مسیح (2000 سال قبل از الکساندر ولتا) آن را اختراع نموده اند.
برای نخستین بار در سال ۱۹۳۸، ویلهلم کونیگ (Wilhelm Konig) باستان شناس آلمانی، در نشریه کاوش و پیشرفت (Forschungen and Fortschritte) در مقالهای خبر از وجود پیلهای اشکانی داد.
ویلهلم کونیگ که ادارهی موزه ملی عراق را بر عهده داشت، هنگام کاوش در منطقه خواجه ربی، یکی از روستاهای نزدیک بغداد (حوالی تیسفون)، به کوزهای سفالی به بلندی ۱۴ سانتیمتر برخورد که استوانهای مسی درون خود داشت و آن استوانه نیز میلهای آهنی را در برگرفته بود و بررسیها از وجود مادهای اسیدی، مانند سرکه در آن ظرف سفالی خبر میداد.
پیش از کونیگ، باستان شناسان دیگری نیز قطعههای شکستهای از این کوزههای راز آمیز را پیدا کرده بودند. با وجود این، تنها او بود که به اهمیت آن ها پی برد و در کشفهای دیگر خود تعداد بیشتری از این باتری ها را پیدا کرد. بررسیها نشان داد که پیشینهی این باطریها به بیش از ۲ هزار سال پیش باز میگردد؛ یعنی زمانی که اشکانیان بر میانرودان (بین النهرین) که از زمان کوروش کبیر، بخشی از خاک ایران بوده است، فرمانروایی میکردند.
اشکانیان سومین سلسله از شاهان بزرگ ایران بودند که از ۲۴۸ سال پیش از میلاد تا ۲۲۴ سال پس از میلاد، امپراتوری شکوهمندی بر پا کرده بودند.
انتشار مقالهی کونیگ، شگفتی باستانشناسان و جهانیان را برانگیخت و هنوز هم پژوهشگرانی پیرامون باتری اشکانیان که به نام باتری پارتی و یا پیل بغداد نیز معروف است، در حال پژوهش می باشند.
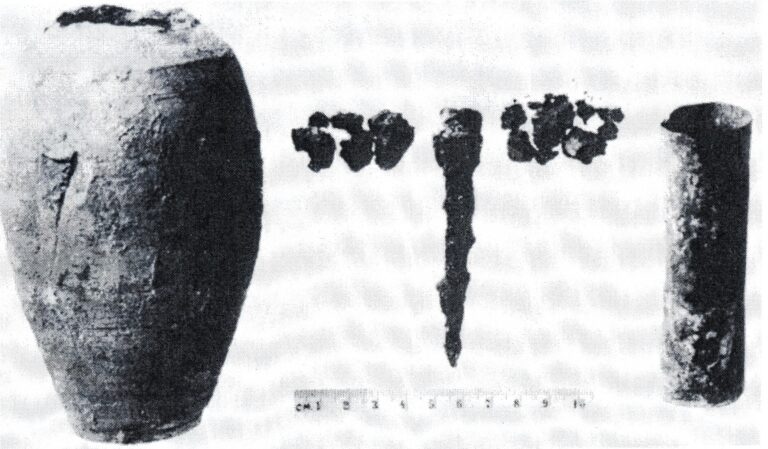
ویژگی های باطری اشکانیان (باطری پارتی)
این شیء در واقع یک کوزه سفالی تخم مرغی شکل به ارتفاع 14 سانتیمتر است که یک میله آهنی به درازای 5/7 سانتیمتر به صورت عمودی، در قسمت میانی آن قرار گرفته که نقش قطب منفی باتری را بر عهده دارد و در اطراف میله آهنی، یک استوانه مسی به طول 8/9 سانتی متر وجود دارد که به کمک قیر در جای خود محکم شده است و نقش قطب مثبت آن را ایفا میکند و دهانه آن نیز، به وسیله قیر کاملا آب بندی شده است.
در مورد الکترولیت نیز به نظر میآید احتمالا از آب نمک، سولفات مس، سرکه، آبلیمو، شراب انگور و یا اسید سیتریک (که در آن دوره شناخته شده بودند) به عنوان الکترولیت استفاده میشده است. به صورت تئوری باتری اشکانیان میتواند 79/0 ولت تولید کند ولی با آزمایشهای انجام گرفته به کمک باتری شبیه سازی شده و به کارگیری محلولهای الکترولیت گوناگون، ثابت شد این باتریها میتوانند ولتاژی معادل 5/0 ولت DC و جریانی چند میلی آمپری را تامین نمایند.
کاربردهای باتری اشکانیان (باتری پارتی)
در این که باتریهای ایرانی الکتریسیته تولید میکنند، شکی نیست، چرا که دانشجویان زیادی در دانشگاههای گوناگون نمونههایی از آن ساختهاند و برق تولید کردهاند. اما اشکانیان از این دستگاه برای چه کاری بهره میگرفتند؟
کشف این باتری فرضیات گوناگونی را برانگیخت. تولید جریان الکتریکی (فرضیه منبع نیرو)، آبکاری طلا و نقره بر دیگر فلزات (فرضیه آبکاری فلزات) و بهره گیری در درمان امراض با شوک الکتریکی (فرضیه کاربرد پزشکی) همگی فرضیاتی بود که در این زمینه مطرح شد. اما با کشف نمونههایی از ظروف، دستبندها و زیورآلات آبکاری شده در اطراف محل کشف این باطریها، فرضیه آبکاری طلا و نقره بر روی دیگر فلزات به نظر قطعی میرسد.
پس از اشکانیان، استفاده از باطری به فراموشی سپرده شد زیرا علمی در این زمینه وجود نداشت.


باتریهای عصر جدید
پس از اشکانیان؛ با تلاشهای گالوانی و ولتا (اواخر قرن هجدهم) باتریهای عصر جدید اختراع شد و سبب تحول شگرفی در جوامع علمی و صنعت الکتریسیته گردید.
لوییجی گالوانی
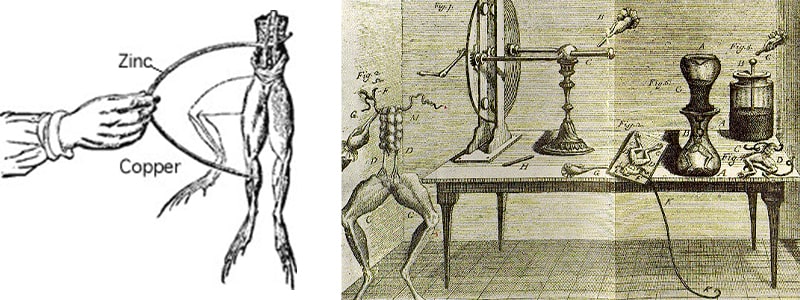
در سال 1791 لوییجی گالوانی دانشمند، پزشک و فیزیک دان سرشناس ایتالیایی قرن هجدهم (1737 تا 1798 میلادی) کشف نمود که اگر ماهیچههای یک قورباغه مرده هدف جرقه یا شوک الکتریکی قرار بگیرد، منبسط شده و شدیداً کشیده میشود و به این ترتیب به صورت تقریبا تصادفی، بیو الکتریسیته را کشف نمود. او همچنین کشف کرد ماهیچهها و سلولهای عصبی الکتریسیته تولید میکنند.
لوییجی گالوانی از پیشگامان تبدیل انرژی شيميايی به انرژی الکتريکی بود.
الکساندر ولتا
در سال 1800، الکساندر ولتا، اولین باتری الکتریکی مدرن را اختراع نمود. ولتا نشان داد زمانی که فلزات و مواد شیمیایی با یکدیگر تماس پیدا کنند، یک جریان الکتریکی تولید میگردد.
مرحله بعد، تولید برق از طریق الکترولیز بود. ولتا در سال 1800 با استفاده از یک سکه مسی، یک سکه نقره و پارچه ابریشمی که در آب نمک غوطه ور شده بود، کشف نمود که یک نیروی جریان پیوسته ممکن است در زمان استفاده از برخی مایعات به عنوان هادی، جهت تسریع فعل و انفعال شیمیایی، بین فلزات اتفاق بیفتد.
ولتا هم چنین کشف نمود که ولتاژ با جمع کردن سلولهای ولتا، افزایش مییابد و این کشف به اختراع پیل ولتا منجر شد. این پیل شامل صفحات متناوبی از مس و روی بود که بین آنها صفحات مقوایی نازک که در محلول نمکی غوطهور بودند قرار داشت.
ویلیام کروکشنک
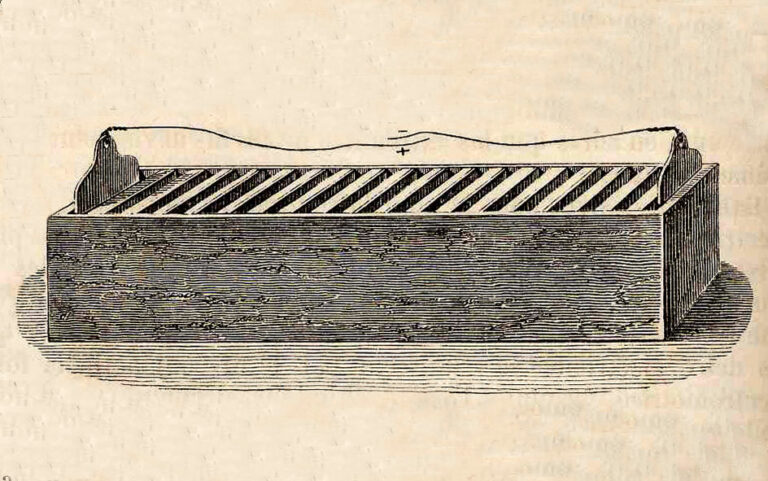
در سال 1802 ، دکتر ویلیام کروکشنک نوعی از باطری را طراحی کرد که میشد آن را به صورت انبوه تولید نمود. کروکشنک صفحات مربعی از مس را که انتهای آنها به یکدیگر لحیم شده بود را با صفحاتی در همان اندازه از روی به طور متناوب درون یک جعبه چوبی بلند که با سیمان بسته شده بود، قرارداد و صفحات فلزی را از درون شیارهای ابتدایی و انتهایی بیرون آورد و جعبه را با الکترولیت پر نمود. این اولین نوع باطری بود که امکان تولید انبوه داشت.
انواع باتری
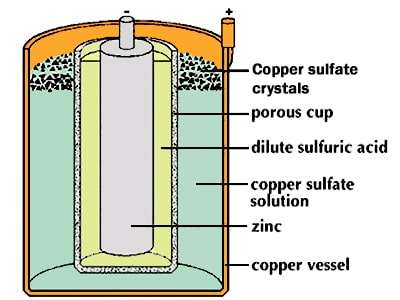
سلول دانیل
این سلول در سال 1836 توسط جان فردریک دانیل (John Frederic Daniell) شیمیدان انگلیسی اختراع شد.
در این سلول مانند پیل ولتا، فلز روی به عنوان آند و مس به عنوان کاتد عمل مینمودند با این تفاوت که دانیل برای افزایش طول عمر باتری و حل مشکل حباب هیدروژن، از دو الکترولیت مجزا استفاده نمود. به این شکل که فلز روی را درون الکترولیت سولفات روی یا اسید سولفوریک رقیق قرار داد و فلز مس با الکترولیت سولفات مس در تماس بود (پوسته خارجی باطری را از جنس مس می ساختند).
از پیل دانیل تا مدتهای طولانی در صنعت تلگراف اروپا استفاده میشد.

باطری سرب اسید
در سال 1859، فیزیکدان فرانسوی گاستون پلانته (Gaston Plante) اولین باتریهای قابل شارژ را بر اساس سیستم اسید و سرب اختراع نمود. این اختراع پس از گذشت بیش از 170 سال، همچنان یکی از محبوبترین انواع باتری میباشد. مدل اولیه این نوع باطری از دو رول مارپیچی از سرب خالص و اکسید سرب که توسط پارچه کتان از هم جدا شده بودند و درون الکترولیت اسید سولفوریک قرار داشتند، تشکیل شده بود.
مدل جدیدی از باتری سرب-اسید در سال 1881 توسط کامیل آلفونس فوره (Camille Alphonse Faure) که یک مهندس فرانسوی بود، ساخته شد. در این مدل، فوره برای غلبه بر محدودیت واکنش شیمیایی و ساخت الکترودهای کارآمدتر، خمیر نازک سرب را بر روی صفحات فلزی قرار داد که این الکترودهای متخلخل امکان تماس بیشتر با الکترولیت را مقدور کرد.


سلول لکلانژه
این سلول اولیه (غیر قابل شارژ) توسط جورجس لاینل لکلانژه ( Georges Lionel Leclanché ) فرانسوی در سال 1866 اختراع شد. ساختمان این سلول شامل یک میله کربن احاطه شده میان پودر دی اکسید منگنز به عنوان کاتد، یک میله فلز روی به عنوان آند و الکترولیت کلراید آمونیوم میباشد.
استفاده از این الکترولیت به جای اسید باعث سبکی و ایمنی بیشتر این سلول گشته بود. این نوع باطری با توجه به قیمت ارزان و سبکی آن، حدود 100 سال بعد، با کمی تغییر در ساختمان آن، در لوازم الکتریکی مخصوصا چراغ قوه و تجهیزات پرتابل استفاده میشد. امروزه این باتری را به نام باتری روی-کربن میشناسیم.

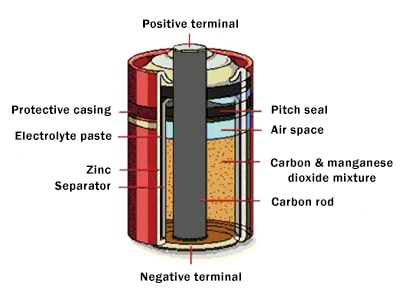
سلول خشک (تکمیل ساختاری سلولهای کربن روی)
سلول لکلانژه بسیار سنگین بود و به راحتی میشکست. ایده اولیه کپسوله سازی باتریها از سال 1881 مورد توجه قرار گرفت ولی ساخت اولین سلولهای خشک توسط کارل گاسنر (Carl Gassner)، شیمیدان شهیر آلمانی، در سال 1887 به انجام رسید.
در این سلولها، الکترود منفی کربن و دیگر عناصر در یک بدنه از جنس “روی” قرار میگرفتند که این بدنه به عنوان قطب مثبت نیز عمل میکرد، الکترولیت جذب یک ماده متخلخل می شد و سلول در قسمت بالا سیلد میگشت. همچنین کلرید روی جهت جلوگیری از خوردگی روی در زمان غیر فعال بودن سلول، به الکترولیت اضافه شد.
قابلیت اصلی این سلولها، حمل بسیار راحت آنها و بدون ریزش الکترولیت بود که به عنوان نمونه اولیه صنعت بزرگ باطریهای خشک معرفی گشت و تاکنون نیز بدون تغییرات چشمگیر در ساختمان آن در حال تولید میباشد.
سلول نیکل کادمیوم
مخترع و مهندس سوئدی ارنست وادمار جانگنر (Ernst Waldemar Jungner) اولین باطریهای نیکل کادمیوم را در سال 1899 اختراع نمود. در این باطری هیدروکسید نیکل به عنوان قطب مثبت، هیدروکسید کادمیوم قطب منفی و هیدروکسید پتاسیم به عنوان الکترولیت عمل مینمایند.
باتری نیکل کادمیوم نخستین باتری استفاده کننده از الکترولیت قلیایی بود. این باتری در آن زمان بسیار قویتر بود و دانسیته انرژی بالاتری نسبت به باتریهای سرب اسید داشت ولی گرانتر بود.
باطری نیکل کادمیوم توانایی شارژ آرام تا سریع یا شارژ پالسی تا یکنواخت را دارد و همچون کارگری ساکت و قوی در شرایط بسیار سخت با کمترین مشکل کار میکند.
در واقع باتری نیکل کادمیوم تنها باتری در بین باتریهای موجود میباشد که میتواند در شرایط کاری بسیار سخت، عملکرد مناسبی داشته باشد. بقیه انواع باطری تخلیه با عمق کم و بارهای متوسط را ترجیح میدهند .
باطری نیکل کادمیوم از لحاظ قیمت اقتصادی ترین باتری نسبت به کارکرد آن میباشد.
در صورت نیاز به مطالعه بیشتر در مورد باطری نیکل کادمیوم به اینجا مراجعه کنید.


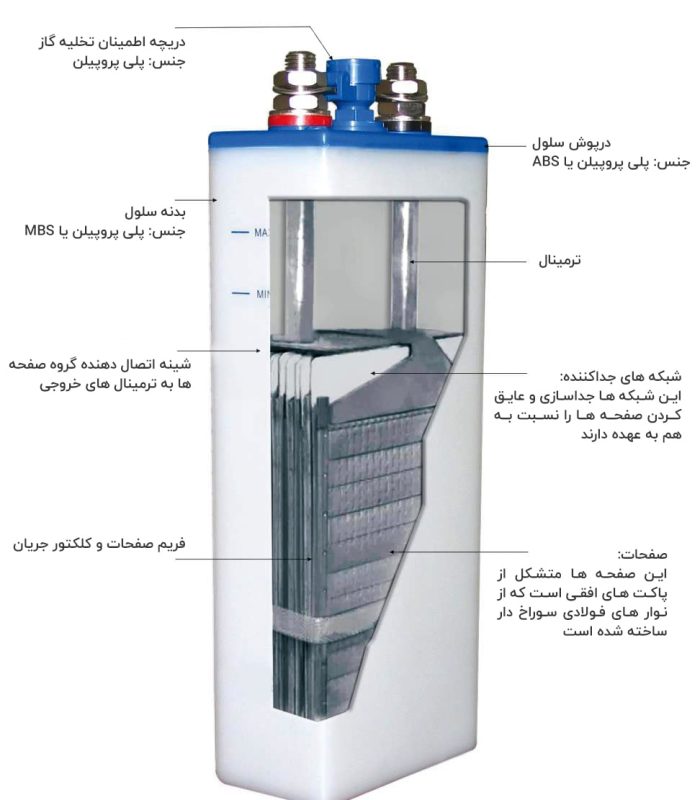
سلول نیکل آهن
اختراع سلولهای نیکل آهن در سال 1905 به نام توماس ادیسون (Thomas Edison) ثبت شد، ولی در واقع مخترع این سلول نیز کسی نبود جز ارنست جانگنر سوئدی. جانگنر گرچه این باطری را در ابتدا اختراع نموده بود ولی با توجه به دانسیته کم انرژی و تولید بیش از حد گاز هیدروژن توجه چندانی به آن ننمود تا ادیسون با اصلاح و توسعه آن، این باتری را به نام خود ثبت نماید.
توانایی اصلی این باتری در مواردی بود که در آن سلولها روزانه شارژ و تخلیه میشدند و ادیسون این نوع باتری را در خودروهای الکتریکی جایگزین باتریهای سرب-اسید نمود که در آن زمان حدود 28 % کل خودروهای ایالات متحده را در بر میگرفت.
در این سلول هیدروکسید نیکل به عنوان کاتد، آهن به عنوان آند و الکترولیت آن هیدروکسید پتاسیم بوده و ولتاژ نامی آن مانند سلولهای نیکل کادمیوم 2/1 ولت میباشد.
در سال 2011 یک محقق آمریکایی موفق شد که یک باتری 85 ساله نیکل آهن را مجددا احیا و آماده بهره برداری نماید که نشان از توانایی و عمر استثنایی باتریهای پایه نیکل دارد.
در دهههای بعدی قرن بیستم و با انفجار تکنولوژی، وجود دو جنگ جهانی اول و دوم و نیاز به کارایی بهتر منابع ذخیره انرژی در جنگ افزارها و تمایل بی حد و حصر انسان به پیشرفت و تعالی، به ناگهان این روند سرعت فزایندهای گرفت؛ به طوری که در قرن بیستم علاوه بر اختراع سلولهایی با تکنولوژی جدید، توسعه و تکمیل اختراعات پیشین و همچنین تجاری سازی آنها، آن چنان باعث افزایش کارایی باطریها گردید که در بسیاری از موارد حتی میتوان میزان اهمیت آن را به اندازه اختراع آنها دانست.
هماکنون در قرن بیست و یک با ورود فناوریهای جدید و نانو، انتظار می رود باطریهای نسل بعد، از نظر کارایی در شرایط مختلف طوری رفتار نمایند که تمام زمینههای ذهنی ما را در خصوص علم فیزیک به چالش بکشند.
برخی اختراعات و اتفاقات مهم باطری در قرن بیستم
- سال 1932: سلولهای نیکل کادمیوم با تکنولوژی سینترد (Sintered Ni-Cd Battery)
در این سال دو مهندس آلمانی شخت (Schlecht) و آکرمان (Ackermann) سلول نیکل کادمیوم با تکنولوژی سینترد را اختراع نمودند که توانایی بسیار زیادی در تخلیه با جریانهای بسیار بالا در زمانهای کوتاه دارد. - سالهای ابتدایی دهه 1940: سلولهای نقره-روی (Silver Zinc)
در طی سالهای ابتدایی دهه 1940 پروفسور فرانسوی هنری آندره (Henri Andre) با تغییر در جداکننده آنها موفق به اصلاح و توسعه اقتصادی این نوع از باطریها گردید. توانایی خارق العاده باتریهای نقره-روی، دانسیته انرژی فوق العاده آنها است. - سال 1947: سلولهای نیکل کادمیوم بسته (Sealed Ni-Cd Battery)
در این سال نیومن (Neumann) فرانسوی موفق به سیلد نمودن باتریهای نیکل کادمیوم گردید که در حال حاضر نیز برای تجهیزات الکترونیکی مختلف مورد استفاده قرار میگیرد. - سال 1949: باتری آلکالاین منگنز
لیو اوری (Lew Urry) در سال 1949 باطریهای کوچک آلکالاین را در آزمایشگاه شرکت Eveready در پارما اصلاح نمود. عملکرد این سلولها 5 تا 8 بار بیشتر از سلولهای کربن-روی بود. این سلولها کماکان در بسیاری از تجهیزات الکترونیکی کوچک از تجهیزات اندازه گیری بسیار پیشرفته تا اسباب بازیها استفاده میگردند. - سال 1950: باتری قلیایی روی اکسید جیوه (Zinc-mercuric oxide alkaline battery)
این باطری توسط روبن (Ruben) که یک مخترع مستقل بود اختراع شد. ترکیبات جیوه در حال حاضر به دلیل مشکلات زیست محیطی دیگر مورد استفاده قرار نمیگیرند. - سال 1960: باطری های دکمه ای (button batteries )
در این سال سلولهای مینیاتوری به نام سلولهای دکمهای با تکنولوژی اکسید نقره برای ساعتها ساخته شد. - دهه 1960: توسعه باتری اولیه آلکالاین ( غیر قابل شارژ ) ( Primary Alkaline Batteries )
شرکت یونیون کارباید (Union Carbide) آمریکا در طی دهه 1960 میلادی ساختار این نوع باتریها را اصلاح نمود. - اواخر دهه 1960: تولید سلول های متال هایدرید (MH)
در این سالها، دانشمندان پی بردند که برخی از ترکیبات فلزی مانند SmCo5 و LaNi5 توانایی جذب و دفع مقدار زیادی هیدروژن را دارند که میتوانند به عنوان یکی از قطبهای منابع ذخیره انرژی استفاده گردند. - ابتدای دهه 1970: اختراع باتریهای غیر قابل شارژ لیتیومی
در سالهای ابتدایی 1970 کمپانیهای مختلف موفق به تولید انواع مختلفی از باطری های غیر قابل شارژ با پایه لیتیوم گردیدند. - دهه 1970: توسعه باتریهای سرب اسید با دریچه قابل تنظیم (Valve Regulated Lead Acid Battery – VRLA)
دهه 1970 به عنوان سالهای طلایی توسعه این نوع باطری یاد میشود که در آن تکنولوژیهای جدید و با قابلیتهای گوناگون در جهت توسعه باتری سرب اسید استفاده گردید. - دهه 1980: اختراع باتریهای قابل شارژ لیتیومی
در این سالها باتری قابل شارژ لیتیومی ساخته شد ولی به دلیل مسائل ایمنی و بی ثباتی ذاتی لیتیوم مخصوصا در زمان شارژ همگی شکست خوردند که باعث شد محققان به سمت سلولهای لیتیوم-یون گرایش پیدا کنند.
سلولهای لیتیوم یون اگرچه دانسیته انرژی کمتری نسبت به فلز لیتیوم داشتند ولی به دلیل ایمنی بیشتر به عنوان جایگزین استفاده شدند. از سلولهای لیتیوم یون، به عنوان سلولهایی با قابلیت پیشرفت یاد میگردد. - سال 199: تولید اقتصادی سلولهای نیکل متال هایدرید (Ni-MH) توسط شرکت SANYO ژاپن
- سال 1991: تولید اقتصادی سلولهای لیتیوم یون (Li Ion) توسط شرکت SONY ژاپن
- سال 1994: تولید اقتصادی سلولهای لیتیوم یون پلیمر (Li Ion Polymer) توسط شرکت Bellcore آمریکا
- سال 1996: تولید اقتصادی سلولهای لیتیوم یون با کاتد منگنز (Li Ion Manganese) توسط شرکت Moli Energy کانادا
- سال 1996: شناسایی سلولهای لیتیوم فسفات (Li-phosphate (LiFePO4)) توسط دانشگاه تگزاس آمریکا
- سال 2002: توسعه سلولهای لیتیوم فسفات با استفاده از تکنولوژی نانو توسط دانشگاههای مونترال، کبک، MIT و دیگران
باتریهای نسل آینده
با پیشرفت فناوری جدید و نانو، این اطمینان وجود دارد که در آیندهای نزدیک سلولهایی با قابلیتهای متفاوت و عجیب تولید شوند که کاملا نیازهای حال حاضر را پاسخ داده و مشکلات باطریهای کنونی را نداشته باشند.
برخی از انواع آنها هم اکنون در مراحل ابتدایی تحقیقات هستند که به آن اشاره میکنیم:
- سلولهایی که میتوان آنها را روی کاغذ پرنیت نمود که میتواند دریچه ای جدید برای باطریهای تجهیزات الکترونیکی قابل حمل باشد.
- پیلهای سوختی به عنوان منابع انرژی قابل حمل مورد استفاده قرار گیرند.
- طراحی و ساخت باطری توسط دانشگاه میزوری ایالات متحده که از فروپاشی ایزوتوپهای رادیواکتیو برای تولید انرژی الکتریکی استفاده مینماید و ابعاد آن به اندازه یک سکه میباشد. این باتری هستهای میتواند یک میلیون برابر باتریهای شیمیایی معمول انرژی الکتریکی تولید کند.
- مهندسان شركت NEC ژاپن موفق به توليد باتری انعطاف پذيری شدند كه ضخامت آن كمتر از يک ميلی متر است و در عرض 30 ثانيه شارژ میشود. از اين باطری در كارت هايی چون كارت های هوشمند RFID استفاده میشود و میتواند بدون نياز به شارژ دوباره تا چندين هفته نيروی كافی اين كارتها را فراهم كند. در اين باتری از نوعی مواد آلی استفاده شده است. برای ساخت اين باطری نوعی پلاستيک از جنس راديكال آلی به شكل يک لايه نازک درآورده شده و از آن به عنوان قطب برق استفاده شده است. ولتاژ اين باتری نازک، مانند باتریهای ليتيومی ۳/۷ولت میباشد. اين باتری از انعطاف پذيری زيادی دارد و میتوان آن را با دست خم کرد.ط
